1. Radio atómico: Corresponde a la mitad de la distancia entre los núcleos de dos átomos vecinos de un mismo elemento que no se encuentran enlazados, o también podemos decir, que es la distancia promedio entre el último electrón del nivel más externo y el núcleo. Los radios atómicos se indican a menudo en angstroms A (10-10m), nanómetros (nm, 10-9 m) picometro (pm, 10-12 m) y Por medio de el es posible determinar el tamaño del átomo.


La variación del radio atómico en la tabla periódica es la siguiente:
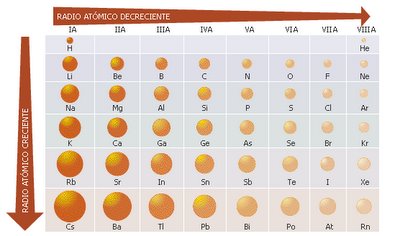
- En un periodo, el radio atómico disminuye de izquierda a derecha, al aumentar el Z.
- En un grupo, en cambio, el radio atómico aumenta de arriba hacia abajo (crece cuando Z aumenta).
2. Energía de ionización (EI)
Potencial de ionización (PI): Es la cantidad de energía necesaria para arrancar o remover un electrón de un átomo neutro en estado fundamental. Es decir, el átomo se convierte en un ión positivo (catión). Esta magnitud puede medirse en kilocalorías por mol (Kcal/mol) y el proceso se representa como sigue:
Esta magnitud puede medirse en kilocalorías por mol (Kcal/mol) y el proceso se representa como sigue:
M + E → M1+ + e- M = metal
En los átomos de los que puede extraer más de un electrón, el proceso de ionización se describe en etapas. Por ejemplo, los tres PI del litio son:
Li → Li+ + e- PI = 124 Kcal/mol
Li+ → Li2+ + e- PI = 1745 Kcal/mol
Li2+ → Li3+ + e- PI = 2822 Kcal/mol
Los PI varían en forma inversa a los radios atómicos. Si es menor el Ra mayor será la atracción existente entre el núcleo y el electrón, por lo tanto, se requerirá una mayor cantidad de energía para remover el electrón. Al contrario, cuanto mayor sea el Ra, menor será la fuerza con que se atraen el núcleo y el electrón, y por tanto, menor será la energía necesaria para extraer dicho electrón.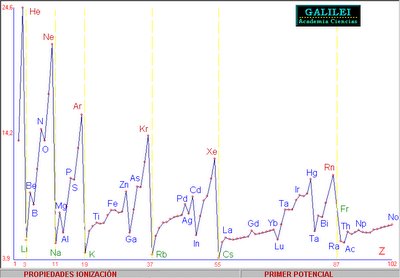
La variación del PI en la tabla periódica es así:
- En un periodo, el PI aumenta de izquierda a derecha.
- En un grupo, el PI aumenta de abajo hacia arriba.
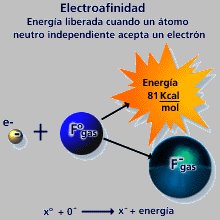
3. Afinidad electrónica o electroafinidad (AE): Es la energía liberada cuando un átomo en estado neutro gana un electrón, para convertirse en un ión negativo (anión). La AE también se expresa en unidades de energía como Kcal/mol y se representa así:
X + e- → X- X = no metal
Cuanta más negativa sea la magnitud de la AE, tanto mayor será la tendencia del elemento a ganar un electrón.
La variación de la AE en la tabla periódica es así:
- En un periodo, la AE aumenta de izquierda a derecha al aumentar el Z.
- En un grupo, la AE disminuye de arriba hacia abajo al aumentar el Z.
4. Electronegatividad (EN): Es la capacidad que tiene un átomo para ganar electrones de otro átomo. Loa átomos que poseen altos valores de EI y AE serán altamente electronegativos y viceversa.
- Linus Pauling determinó escalas de EN que varían del 0,7 al 4,0.
- Para los gases nobles la EN es 0 por ser estables.
La variación de la EN en la tabla periódica es así: - En un periodo aumenta hacia la derecha.
- En un grupo aumenta hacia arriba.

35 comentarios
gracias profesor jorge diaz por la pag ya que tenemos prueba mañana y esto nos ayuda a preparanos mejor
aunque no del todo
atte su alumna
c.f
profe qliao viejo de mierda pasao a caca jorge qliao
La informacion es muy buena; pero me gustaria conocer mas del tema, por ejemplo: El radio atomico que tienen determinados los elementos en picometro, sus valores de energia y su electroafinidad. Gracias. Paola
oiga profe, tengo una pregunta que me gustaria que me respondiese ojala antes del martes 2 sep. ya que tengo una prueba.
¿por q el tamaño de los elementos q constituyen un grupo en la Tabla Periodica aumenta de arriba hacia abajo, en cambio, en los periodos lo hace de derecha a izquierda?
(estudiando)
:
¿por q las propiedades periodicas son periodicas?
:)
Gracias! esta muy buena la info y me sirve mucho... chau!
ta weno weno esto
=)
grazia profe q dios padre todo poderoso lo aco`pañe en todo lugar y recuerde q nunka esta solo siempre esta cn el dios todo poderoso
se despide atte
matias
q dios lo bendiga mucho y a su familia
viejo culia pasao a caca el weon y la tiene corta el viejo feo de mierda jorje culias weno pa la tula
con amor tu ermana sapo culiao
muy buena su pagina, de verdad me ayudo a comprender cuidese
me rrreeeeeeee ayudaste para mi prueba de mañana,
muchas graciaas !
oiga profe zabe qe no se cmo se saqan los calculos quimicos ? zi podria poner ahi i enseñar ademas en la pag 2 medio le falta informacionde los enlace etc... adios grasias
gracias n.n
Pusha pero quiero el orden de todas las propiedades periodicas po 77, pa adonde aumenta, de izquierda a derecha, y de arriba o abajo, del centro hacia afuera, etc. no me sirvio pana la pagina 77
profesor le doy las gracias por aber acho esta pagina, con la cual yo logre entender mucho mas la quimica (aunque le pediria que porfavor pusiera ejercicios resueltos para que se pueda entender mejor algunos calculos quimicos), a pesar de que yo no soy de 2do medio,pero si de la universidad, igual sirve de mucho su pagina, para los que nunca logramos entenderle a los profes que algunavez nos hicieron clases.
con el mas devido respeto, muchas gracias...
tienes un problema serio con los grupos y periodos los periodos son hacia abajo y los grupos van arriba tienes todo cambiado..
terrible hueono esto xau xD
grasia profe me ayudo pa la pruea de mañana pero toy cagao = pero filo cage no mas xaouuuuu
matias
grasia xe sos agallao xe
:O xD
que infomacion tan incompleta da lastima
k mierda!
Don Jorge, si no le paga a Don Corleone....... usted sabe..
Don Jorge, si no le paga a Don Corleone....... usted sabe..
la información esta mas o menos pero aun asi tenia lo q me faltaba asi q no m quejo
esta bien con graficos y todo, esta bien :)
Exente si no fuera por esta pagina no se que pasaría me ayudo mucho con un trabajo lo felicito
Cómo cambia el radio atómico de arriba hacia abajo en un grupo?
bmo no se nada pero entre y me parece super hiper mega mala
ok
bye
hola profesor la verdad que no entendi nada y tengo que rendir el 20 de febrero fq y el profe me va a tomar 10 elementos de la tabla periodica por eje aro nikel cinic y de esos elementos me va a aser un cuadro que tenga que decir el pi,e-.a° ,p,g varias cosas asi pero no me acuerdo mas de esas y no se como ago aver que cosas son esas osea como calcularlas y no se que significa pi a e por que en la tabla no me dice eso solo dice grupo y peiodo y los eletrones
y la cantidad de atomos
energia de ionizacion es asi pero te falto poner que es en estado gaseoso. pequeño gran detalle.
Alguien aquí juega clash of clans
O clash royale respondan para unirme a un clan
LOL
elpapi
No Malparida
no entendi
Publicar un comentario